Возможные валентности галогенов с точки зрения строения атома :
Для галогенов характерна , переменная валентность: I, III, V, VII. Только фтор проявляет постоянную валентность. Строение внешнего электронного слоя галогенов ...ns2 np5, электронно-графическая формула ...
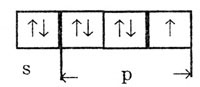
Так как у всех галогенов в нормальном состоянии один неспаренный электрон, то они могут образовать одну связь, то есть одновалентны. Переменная валентность объясняется возбуждением атома, переходом электронов на свободные энергетические ячейки р-подуровня и увеличением числа неспаренных электронов.
Строение внешнего электронного слоя атомов галогенов в возбужденном состоянии:
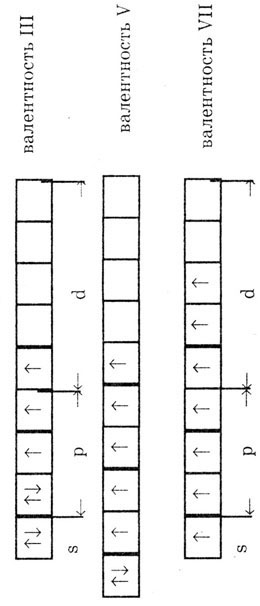
Фтор находится во втором периоде (n = 2), поэтому у него на втором энергетическом уровне только два подуровня: s и р, подуровень d отсутствует. Этим объясняется постоянная валентность фтора, равная единице.